Bakteriophagen
Der gezielte Einsatz von Bakteriophagen könnte Antibiotika komplett ersetzen. Dabei bestünde nicht einmal das Risiko einer Nebenwirkung für den Menschen, da sie ausschließlich auf Bakterien gehen können.
- Phagen töten schädliche Bakterien schneller und sicherer als Antibiotika.

Zu beachten ist, dass nicht jede Phage jedes Bakterium tötet, vielmehr gibt es für jedes Bakterium eine Phage, mit der diese auch kompatibel ist.
Würde man im Krankenhausbereich das Wissen der Lebensmittelwirtschaft einsetzen, könnte man dort Bakteriophagen gegen Antibiotika resistente Keime einsetzen, um sie, wie beispielsweise die Staphylococcus aureus (MRSA) erfolgreich zu bekämpfen, die heute noch für viele Infektionen und Todesfälle verantwortlich sind.
Warum gibt es sie nicht längst in deutschen Apotheken, so wie beispielsweise in Georgien? Genau! Wieder das alte Lied der Gewinnspanne. Es ist was natürliches, ist nicht patentierbar, ist leicht verfügbar, auch noch nebenwirkungsfrei ... Ein Graus für jeden Hersteller von Medikamenten.
| Organismus | Größe (Durchmesser) | Größe im Vergleich zum Bakterium (%) |
|---|---|---|
| Bakterium | etwa 1 - 10 µm | 100% |
| Virus | typischerweise 20 - 300 nm | 0.2% - 30% |
| Bakteriophage | etwa 20 - 200 nm | 0.2% - 20% |
Anwendungsgebiete für Phagen
Lebensmittelindustrie
- Lebensmittelsicherheit: Kontrolle und Reduzierung von pathogenen Bakterien wie *Salmonella*, *E. coli* und *Listeria monocytogenes* in Lebensmitteln.
- Oberflächenbehandlung: Anwendung von Phagen auf Verpackungen und Produktionsoberflächen zur Verhinderung der Kreuzkontamination.
- Haltbarkeitsverlängerung: Einsatz von Phagen zur Verlängerung der Haltbarkeit von Lebensmitteln durch Verhinderung von bakteriellen Verderb.
Medizin
- Phagentherapie: Behandlung von bakteriellen Infektionen, insbesondere bei Antibiotika-resistenten Stämmen wie *Methicillin-resistentem Staphylococcus aureus (MRSA)*.
- Diagnostik: Entwicklung von phagenbasierten Tests zur schnellen Identifikation von Krankheitserregern.
- Wundheilung: Verwendung von Phagen zur Behandlung chronischer Wunden und Hautinfektionen.
Umweltschutz
- Abwasserbehandlung: Einsatz von Phagen zur Bekämpfung von pathogenen Bakterien in Abwasserbehandlungsanlagen.
- Bioremediation: Verwendung von Phagen zur Reinigung von kontaminierten Böden und Gewässern, indem sie spezifische Bakterien abbauen.
Landwirtschaft
- Tiergesundheit: Anwendung von Phagen zur Kontrolle von bakteriellen Infektionen bei Tieren, wie z.B. in der Aquakultur zur Bekämpfung von *Vibrio*-Infektionen.
- Pflanzenschutz: Einsatz von Phagen zur Bekämpfung von Phytopathogenen, die Pflanzenkrankheiten verursachen.
Biotechnologie
- Gentechnik: Nutzung von Phagen als Werkzeuge für die Übertragung von genetischem Material in Bakterien, z.B. in der Phagen-Display-Technologie zur Identifizierung von Proteinen oder Antikörpern.
- Phagen-Sortierung: Selektive Isolierung von Bakterien durch phagenbasierte Methoden.
Forschung
- Mikrobiom-Forschung: Untersuchung der Rolle von Phagen im Mikrobiom und ihrer Wechselwirkungen mit Bakterien.
- Evolutionäre Studien: Erforschung der Evolution von Phagen und ihrer Anpassungen an verschiedene Bakterien.
Phagen-Biopestizide
- Pestizidindustrie: Entwicklung von phagenbasierten Biopestiziden zur Bekämpfung von Schädlingen und Schaderregern in der Landwirtschaft.
Klinische Studien und Impfstoffe
- Impfstoffentwicklung: Nutzung von Phagen als Träger für die Herstellung von Impfstoffen und zur Immunisierung gegen bestimmte Pathogene.
Phagen - für Lebensmittelchemiker ein alter Hut
Bakteriophagen, oft einfach als Phagen bezeichnet, sind Viren, die gezielt Bakterien infizieren und abtöten können. In der Lebensmittelindustrie werden sie schon seit 1930 eingesetzt, da sie als effektive Werkzeuge zur Kontrolle von bakteriellen Kontaminationen in Lebensmitteln dienen. Die Forschung und Anwendung von Phagen in diesem Bereich haben sich in den letzten Jahrzehnten erheblich weiterentwickelt.
In der Lebensmittelproduktion sind Phagen von großem Interesse, weil sie auf spezifische Krankheitserreger abzielen, ohne die nützlichen Mikroben oder die Qualität der Lebensmittel zu beeinträchtigen. Beispielsweise werden Phagen verwendet, um gefährliche Bakterien wie Salmonella, E. coli und Listeria monocytogenes zu bekämpfen, die in rohen Fleischprodukten, Milchprodukten und anderen Lebensmitteln vorkommen können. Diese Phagen können entweder als direktes Additiv in Lebensmittelproduktionsprozesse integriert oder als Prävention durch Oberflächenbehandlung von Lebensmittelverpackungen eingesetzt werden.
Der Vorteil von Phagen liegt in ihrer hohen Spezifität; sie infizieren nur bestimmte Bakterienstämme und lassen andere Bakterienarten oder die menschliche Mikrobiota unberührt. Dies ermöglicht eine zielgerichtete Bekämpfung von schädlichen Bakterien, ohne das allgemeine Mikrobiom der Lebensmittel oder ihre ernährungsphysiologischen Eigenschaften negativ zu beeinflussen. Darüber hinaus tragen Phagen zur Reduzierung der Notwendigkeit von Antibiotika in der Lebensmittelproduktion bei, was besonders wichtig ist, um die Entstehung und Verbreitung von antibiotikaresistenten Bakterien zu verhindern.
In der Praxis bedeutet dies, dass die Verwendung von Phagen in der Lebensmittelindustrie nicht nur zur Erhöhung der Lebensmittelsicherheit beiträgt, sondern auch zu einer nachhaltigeren und umweltfreundlicheren Produktion führt.
Vorteile des medizinischen Einsatzes von Bakteriophagen:
- keine Resistenz möglich
- natürlich und verträglich
- schnelle und sichere Art gegen Bakterien erfolgreich vorzugehen
Eine Bakteriophagentherapie beginnt mit der genauen Diagnose der bakteriellen Infektion und der Isolation spezifischer Phagen, die gegen den identifizierten Erreger wirksam sind. Diese Phagen werden gereinigt, vermehrt und in einer geeigneten Formulierung verabreicht, je nach Art der Infektion, beispielsweise oral, topisch oder intravenös. Während der Therapie wird der Patient überwacht und die Behandlung bei Bedarf angepasst, um die Wirksamkeit zu maximieren.
Nebenwirkungen sollten praktisch nicht Auftreten, da die Bakteriophagen i.d.R. nur auf bestimmte Bakterien gehen. Sie fressen die Bakterien auf und verhungern letztlich, sterben und werden vom Organismus ausgeschieden.
In der Natur
Man findet sie in der Natur meist in verschmutzten Gewässern, wie zum Beispiel im Ganges in Indien, weshalb dort wohl auch das Gerücht entstand, dieses "heilige" Wasser hätte eine heilende Wirkung. Bereits 1896 wurde dies bei einer Cholera-Epidemie erfolgreich eingesetzt.
Gleiches wurde auch schon mit Diphtherie-kranken Kindern und mit dem schmutzigen Wasser aus der Seine wiederholt, wobei dabei die Kinder praktisch über Nacht Genesung erfuhren.
Geschichtlich
Bevor man Antibiotika entdeckte, wurde die Erkenntnis über das Flusswasser gegen Infektionskrankheiten eingesetzt. Es wurde dann, um ein vermarktungsfähiges Mittel anbieten zu können, das Wasser weitgehend aufbereitet, um möglichst nur noch Phagen im Wasser zu lassen. Doch dadurch meinten die damaligen Fachleute zu erkennen, dass es sich dabei nur um schlichtes Wasser handle, da man die Phagen mit bloßem Auge nicht sehen kann.
So füllten sie einfaches Wasser ab und boten dies bei schweren Infektionskrankheiten teuer zur Heilung an. Eine Wirkung blieb dabei natürlich aus. Der Knockout kam am Ende mit der Idee, das Wasser vorher noch mit Desinfektionsmittel zu behandeln. Dadurch kam es zum Verruf bis Antibiotika an die freigewordene Stelle traten.
Man kennt Phagen und Ihre effizienten Eigenschaften schon lange, wie z.B.:
Bakteriophagen von schmutzigem Wasser aus der Seine bei Diphtherie-kranken Kindern

Zeit und Ort: Frühes 20. Jahrhundert, Paris, Frankreich.
Details: Während des frühen 20. Jahrhunderts entdeckte Felix d'Herelle, ein französischer Mikrobiologe, dass das schmutzige Wasser der Seine natürliche Bakteriophagen enthielt. Diese Phagen, die Bakterien infizieren und abtöten können, erwiesen sich als nützlich im Kampf gegen bakterielle Infektionen. D'Herelle isolierte diese Bakteriophagen und erkannte ihr Potenzial zur Behandlung von Infektionskrankheiten wie Diphtherie.
In einem bemerkenswerten Experiment behandelte d'Herelle Diphtherie-kranke Kinder mit diesen aus dem Seine-Wasser isolierten Bakteriophagen. Die Ergebnisse waren beeindruckend: Die Kinder erfuhren oft eine schnelle Genesung, manchmal bereits über Nacht. Diese frühe Anwendung von Bakteriophagen markierte einen wichtigen Schritt in der medizinischen Forschung und eröffnete neue Möglichkeiten zur Behandlung von bakteriellen Infektionen.
Die Verwendung von schmutzigem Wasser aus der Seine als Quelle für Bakteriophagen demonstrierte die natürlichen Vorkommen dieser Viren und ihre potenzielle Anwendung in der Medizin. D'Herelles Arbeit trug dazu bei, die Grundlage für die spätere Erforschung und Entwicklung der Phagentherapie zu legen, die als Alternative zu Antibiotika angesehen wird.
Bakteriophagen-Einsatz während der Cholera-Epidemie 1892 in Hamburg
Zeit und Ort: Im Jahr 1892 während einer verheerenden Cholera-Epidemie in Hamburg.
Details: Die Cholera-Epidemie von 1892 war eine der schwersten gesundheitlichen Krisen in Hamburgs Geschichte. Max von Pettenkofer, ein angesehener deutscher Bakteriologe und Hygieniker, spielte eine kontroverse Rolle in der Bekämpfung der Epidemie. Pettenkofer, der für seine Theorie des "Miasmas" bekannt war, glaubte, dass Epidemien durch schlechte Luftqualität und Umweltbedingungen verursacht wurden.
Während der Epidemie propagierte Pettenkofer die Idee, dass das Flusswasser der Isar in München heilende Eigenschaften besaß und forderte, dieses Wasser zur Bekämpfung der Cholera in Hamburg einzusetzen. Er glaubte, dass die "heilende Kraft" des Wassers die Ausbreitung der Krankheit stoppen könne. Trotz seiner wissenschaftlichen Stellung und seiner Überzeugung wurden seine Vorschläge nicht effektiv umgesetzt und trugen nicht zur Eindämmung der Epidemie bei. Stattdessen verstärkte die falsche Anwendung seiner Theorie und die unsachgemäße Nutzung von Flusswasser als Heilmittel die Verwirrung und führte zu einer verzögerten Reaktion der Gesundheitsbehörden.
Die Cholera-Epidemie von 1892 in Hamburg diente als Wendepunkt in der Hygiene- und Epidemiologiegeschichte, indem sie die Notwendigkeit wissenschaftlich fundierter und evidenzbasierter Ansätze zur Bekämpfung von Infektionskrankheiten unterstrich.
Forschung von Felix d'Herelle und die Anwendung von Bakteriophagen in Deutschland

Zeit und Ort: Während des frühen 20. Jahrhunderts, hauptsächlich am Institut Pasteur in Paris, wo Felix d'Herelle arbeitete, aber mit enger Zusammenarbeit mit deutschen Wissenschaftlern und Forschungseinrichtungen.
Details: Felix d'Herelle, ein französischer Mikrobiologe, gilt als einer der Pioniere der Bakteriophagenforschung und -therapie. Er entdeckte Bakteriophagen, Viren, die Bakterien infizieren und abtöten können, und erkannte ihr Potenzial als alternative Behandlungsmethode für bakterielle Infektionen. D'Herelle führte umfangreiche Forschungen durch, um die Natur und Anwendungen von Bakteriophagen zu verstehen, und entwickelte sie als gezielte Therapieoption gegen bestimmte bakterielle Krankheitserreger.
Obwohl d'Herelle hauptsächlich am Institut Pasteur in Paris arbeitete, pflegte er auch enge Verbindungen zu deutschen Wissenschaftlern und Forschungseinrichtungen. Diese Zusammenarbeit war besonders wichtig für die frühe Entwicklung der Phagentherapie, da Deutschland zu dieser Zeit eine führende Rolle in der medizinischen Forschung und Mikrobiologie spielte.
Die Arbeit von Felix d'Herelle war wegweisend und beeinflusste die Forschung und Entwicklung von Bakteriophagen weltweit. Seine Entdeckungen markierten einen Meilenstein in der Geschichte der Medizin, indem sie eine neue Behandlungsmethode gegen bakterielle Infektionen eröffneten und ein alternatives Werkzeug zur Antibiotikatherapie darstellten.
Diese historischen Ereignisse veranschaulichen die frühe Nutzung von Bakteriophagen in Deutschland und ihre Auswirkungen auf die medizinische Forschung und Praxis sowie die Herausforderungen und Missverständnisse im Umgang mit epidemischen Krankheiten wie der Cholera im 19. Jahrhundert.
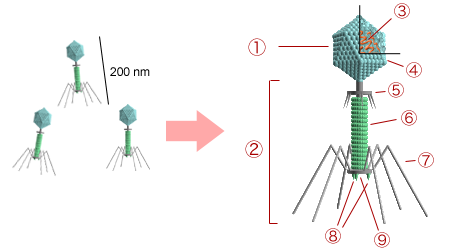
Aufbau einer Phage
- Head
- Tail
- Nucleic acid
- Capsid
- Collar
- Sheath
- Tail fiber
- Spikes
- Baseplate
Illustrative Darstellung des lytischen Zyklus einer Bakteriophage.
- A) Die Phage besitzt Bindungsproteine (dargestellt als rosa Kugeln), die spezifische Membranrezeptoren (rote Rezeptoren) auf dem Zielbakterium erkennen.
- B) Nach der Erkennung des Rezeptor-Ligand-Komplexes haftet der Bakteriophage an der Membran des Bakteriums an und setzt dann sein genetisches Material frei.
- C) Das in die Zelle eingeführte genetische Material wird von bakteriellen Proteinen erkannt, die die viralen Gene transkribieren und übersetzen, was zur Synthese neuer Bakteriophagen führt.
- D) Neben den Bakteriophagen selbst enthält das virale genetische Material auch Gene, die destruktive Enzyme kodieren, die die Wirtszelle lysieren können. So werden die neu synthetisierten Bakteriophagen freigesetzt, was einen neuen Infektionszyklus einleitet.
Liste bekannter Bakteriophagen und ihre Einsatzgebiete in der Medizin
Lytic VRE Phage
- Wirt: Enterococcus faecium (Vancomycin-resistente Enterokokken)
- Einsatzgebiet: Medizinische Anwendungen; Behandlung von Vancomycin-resistenten Infektionen.
Listeria Phage A511
- Wirt: Listeria spp.
- Einsatzgebiet: Lebensmittelindustrie; Kontrolle von Listeria monocytogenes in Lebensmitteln.
Staphylococcus Phage K
- Wirt: Staphylococcus aureus (einschließlich MRSA-Stämme)
- Einsatzgebiet: Medizinische Anwendungen; Behandlung von Staphylococcus-Infektionen, einschließlich Methicillin-resistenter Staphylococcus aureus (MRSA).
Salmonella Phage Felix O1
- Wirt: Salmonella spp.
- Einsatzgebiet: Lebensmittelindustrie und Medizin; Kontrolle und Behandlung von Salmonella-Infektionen.
Mycobacteriophage D29
- Wirt: Mycobacterium tuberculosis
- Einsatzgebiet: Forschung und medizinische Anwendungen; Studien zur Tuberkulose und zur Entwicklung neuer Therapien.
Pseudomonas Phage PaP1
- Wirt: Pseudomonas aeruginosa
- Einsatzgebiet: Medizinische Anwendungen; Behandlung von Infektionen durch Pseudomonas aeruginosa, insbesondere bei Patienten mit Mukoviszidose.
Klebsiella Phage KP34
- Wirt: Klebsiella pneumoniae
- Einsatzgebiet: Medizinische Anwendungen; Behandlung von Klebsiella-Infektionen, einschließlich Antibiotika-resistenter Stämme.
Escherichia Phage T4
- Wirt: Escherichia coli (E. coli)
- Einsatzgebiet: Medizinische Anwendungen; Behandlung von Infektionen durch pathogene E. coli-Stämme.
Acinetobacter Phage AB1
- Wirt: Acinetobacter baumannii
- Einsatzgebiet: Medizinische Anwendungen; Behandlung von Infektionen durch Acinetobacter baumannii, insbesondere Antibiotika-resistenter Stämme.
Woher bekommt man Bakteriophagen
Bakteriophagen nicht in Deutschland erhältlich
In Deutschland sind Bakteriophagen derzeit nicht als reguläre Arzneimittel zugelassen und daher nicht in Apotheken erhältlich. Offizielle Gründe dafür sind:
- Regulatorische Hürden: Bakteriophagen sind nicht als konventionelle Arzneimittel zugelassen, da umfangreiche klinische Studien zur Sicherheit und Wirksamkeit fehlen.
- Fehlende Zulassung: Ohne spezifische Zulassung als Arzneimittel können Bakteriophagen nicht in den Apothekenvertrieb gelangen.
- Komplexität und Individualität: Bakteriophagen erfordern möglicherweise eine individuelle Auswahl und Anpassung, was Standardisierung und Massenproduktion erschwert.
- Fehlende Standardisierung: Die Produktion von Bakteriophagen erfordert spezielle technische und regulatorische Anforderungen, die derzeit nicht standardisiert sind.
- Forschungsstatus: Bakteriophagen befinden sich noch im Forschungs- und Entwicklungsstadium und sind nicht für breite klinische Anwendungen zugelassen.
In Zukunft könnten sich diese Bedingungen ändern, wenn mehr Daten über die Sicherheit und Wirksamkeit gesammelt werden und regulatorische Rahmenbedingungen für ihre Nutzung geschaffen werden.
Erhältlichkeit in Nachbarländern
Bakteriophagen sind derzeit in folgenden Ländern tatsächlich in Apotheken oder für medizinische Anwendungen erhältlich:
- Georgien: Bakteriophagen sind als Arzneimittel zugelassen und weit verbreitet in Apotheken und medizinischen Einrichtungen erhältlich.
- Polen: In Polen werden Bakteriophagen in spezialisierten Kliniken und Krankenhäusern zur Behandlung von Infektionen eingesetzt. Es gibt spezialisierte Zentren, die Bakteriophagen für therapeutische Zwecke produzieren und anwenden.
- Russland: Bakteriophagen sind in Russland als Arzneimittel zugelassen und können in Apotheken und medizinischen Einrichtungen erworben werden.
Diese Länder haben eine längere Geschichte in der Nutzung und Forschung von Bakteriophagen und verfügen über spezifische gesetzliche Rahmenbedingungen, die ihre Verwendung als Therapie unterstützen.
Der Import von Bakteriophagen aus beispielsweise Georgien nach Deutschland erfordert spezielle Genehmigungen und muss den deutschen Arzneimittel- und Gesundheitsvorschriften entsprechen. Eine detaillierte Abstimmung mit den zuständigen Behörden und Fachexperten ist notwendig, um die gesetzlichen Anforderungen zu erfüllen. Sprich, es ist für die alltägliche Anwendung praktisch nicht möglich.
Isolierung und Züchtung von Bakteriophagen
Die hier beschriebenen Verfahren sind stark vereinfacht und setzen grundlegende Kenntnisse in Mikrobiologie und Labortechniken voraus. Für eine detaillierte und präzise Anleitung sollten spezifische wissenschaftliche Protokolle und Sicherheitsrichtlinien befolgt werden.
Isolierung von Bakteriophagen aus Wasser
Materialien:
- Wasserprobe aus einer natürlichen Quelle (z.B. Fluss, See, Abwasser)
- Sterile Behälter
- Zentrifuge
- Filter (0,22 µm)
- Nährmedium für Bakterien (z.B. LB-Bouillon)
- Zielbakterienkultur (Bakterien, die von den Phagen infiziert werden sollen)
- Agarplatten
Schritte:
- Probenahme: Sammeln Sie Wasserproben aus einer natürlichen Quelle. Stellen Sie sicher, dass die Behälter steril sind, um Verunreinigungen zu vermeiden.
- Zentrifugation: Zentrifugieren Sie die Wasserprobe bei hoher Geschwindigkeit (etwa 10.000 x g) für 10-15 Minuten, um feste Partikel und größere Organismen abzutrennen.
- Filtration: Filtern Sie die überstehende Flüssigkeit durch einen 0,22 µm Filter, um Bakterien und andere größere Mikroorganismen zu entfernen, während Bakteriophagen durch den Filter passieren können.
- Anreicherung: Geben Sie die gefilterte Lösung in ein steriles Gefäß mit einer kleinen Menge Nährmedium und einer Kultur der Zielbakterien. Inkubieren Sie diese Mischung über Nacht bei geeigneter Temperatur (meist 37°C), um die Phagenpopulation zu vermehren.
- Phagen-Isolierung: Nach der Inkubation zentrifugieren Sie die Mischung erneut und filtern die überstehende Flüssigkeit durch einen 0,22 µm Filter. Diese Lösung enthält die angereicherten Bakteriophagen.
- Phagen-Überprüfung: Tropfen Sie die Phagenlösung auf Agarplatten, die mit der Zielbakterienkultur bedeckt sind. Nach weiterer Inkubation bilden sich klare Zonen (Plaques) auf den Platten, die auf das Vorhandensein von Bakteriophagen hinweisen.
Züchtung von Bakteriophagen
Materialien:
- Bakteriophagen-Stamm (aus den isolierten Plaques)
- Zielbakterienkultur
- Nährmedium (LB-Bouillon)
- Erlenmeyerkolben oder andere geeignete Kulturgefäße
- Schüttelinkubator
Schritte:
- Vorbereitung der Bakterienkultur: Bereiten Sie eine frische Kultur der Zielbakterien in LB-Bouillon vor. Inkubieren Sie diese bei 37°C, bis sie die log-Phase des Wachstums erreicht haben (typischerweise eine OD600 von 0,4-0,6).
- Infektion der Bakterienkultur: Fügen Sie eine kleine Menge der Phagenlösung (z.B. 1 ml) zu 50 ml der Bakterienkultur hinzu.
- Inkubation: Inkubieren Sie die Mischung bei 37°C in einem Schüttelinkubator (ca. 100-200 Umdrehungen pro Minute) für mehrere Stunden, bis die Kultur klar wird. Die Klarheit zeigt, dass die Bakterien von den Phagen abgetötet wurden und die Phagen sich vermehrt haben.
- Phagen-Ernte: Zentrifugieren Sie die Kultur bei hoher Geschwindigkeit (10.000 x g) für 10-15 Minuten, um Zelltrümmer zu entfernen.
- Filtration: Filtern Sie die überstehende Flüssigkeit durch einen 0,22 µm Filter, um die Phagen von restlichen Bakterien und Zelltrümmern zu trennen.
- Lagerung: Lagern Sie die gefilterte Phagenlösung in sterilen Behältern bei 4°C für den kurzfristigen Gebrauch oder frieren Sie sie bei -80°C für die Langzeitlagerung ein.
Sicherheitshinweise
- Arbeiten Sie immer unter sterilen Bedingungen, um Kontaminationen zu vermeiden.
Arbeiten unter sterilen Bedingungen ist unerlässlich, um die Verunreinigung von Bakteriophagenpräparaten mit unerwünschten Mikroorganismen zu verhindern. Kontaminationen können die Wirksamkeit der Therapie beeinträchtigen, da fremde Bakterien oder Viren die Phagen beeinflussen oder den Patienten infizieren könnten. Sterilität stellt sicher, dass die Phagenpräparate rein und sicher für die Behandlung sind, wodurch das Risiko von Infektionen und Komplikationen minimiert wird.
- Tragen Sie geeignete Schutzausrüstung, einschließlich Laborkittel, Handschuhe und Schutzbrille.
Das Tragen geeigneter Schutzausrüstung schützt sowohl das medizinische Personal als auch die Patienten. Laborkittel und Handschuhe verhindern die Übertragung von Krankheitserregern auf und von der Haut des Personals, während Schutzbrillen die Augen vor Spritzern von biologischen Materialien schützen. Diese Ausrüstung reduziert das Risiko von Infektionen und Kontaminationen und sorgt für eine sichere Handhabung der Phagenpräparate.
- Entsorgen Sie alle biologischen Abfälle gemäß den geltenden Vorschriften.
Die ordnungsgemäße Entsorgung biologischer Abfälle ist entscheidend, um die Ausbreitung von Krankheitserregern und Umweltkontaminationen zu verhindern. Unsachgemäß entsorgte Abfälle können Infektionskrankheiten verbreiten und die Gesundheit der Allgemeinheit gefährden. Durch die Einhaltung der geltenden Vorschriften wird sichergestellt, dass alle biologischen Abfälle sicher und effizient entsorgt werden, wodurch die Umwelt und die öffentliche Gesundheit geschützt werden.
Quellen
- Siehe:
- Wikipedia
- weiter zur PDF von fraunhofer.de
- Bakteriophagen - natürlicher Ersatz für Antibiotika und Desinfektion? weiter zum Youtube Video